Sperimentazioni cliniche certificate: prove digitali per trial e monitoraggio
Certifica la documentazione dei trial clinici alla fonte con firma digitale e marca temporale per dati conformi a GCP e ALCOA+.
La sperimentazione clinica richiede una documentazione rigorosa e tracciabile in ogni fase del trial. Il Regolamento UE 536/2014 e le linee guida ICH E6(R3) impongono standard elevati per la raccolta, la conservazione e la verificabilità dei dati clinici, secondo i principi ALCOA+.
Fotografie di attività di sito, documenti sorgente, registrazioni di eventi avversi e verifiche di accountability del farmaco sperimentale spesso mancano di garanzie di autenticità e collocazione temporale certa. TrueScreen certifica ogni evidenza digitale al momento della raccolta con firma digitale e marca temporale, garantendo integrità, tracciabilità e conformità regolatoria fino dalla fonte.
Settore
Farmaceutico, ricerca clinica, CRO
Funzione aziendale
Operazioni cliniche, assicurazione della qualità, affari regolatori
Processo chiave
Documentazione e monitoraggio sperimentazioni cliniche
Contenuti certificati
Foto, video, documenti sorgente, report di monitoraggio, registrazioni, checklist
Output
Documentazione e reportistica certificata con valore legale
Modalità di adozione
App / Web / API / SDK
Esigenze

Soluzione
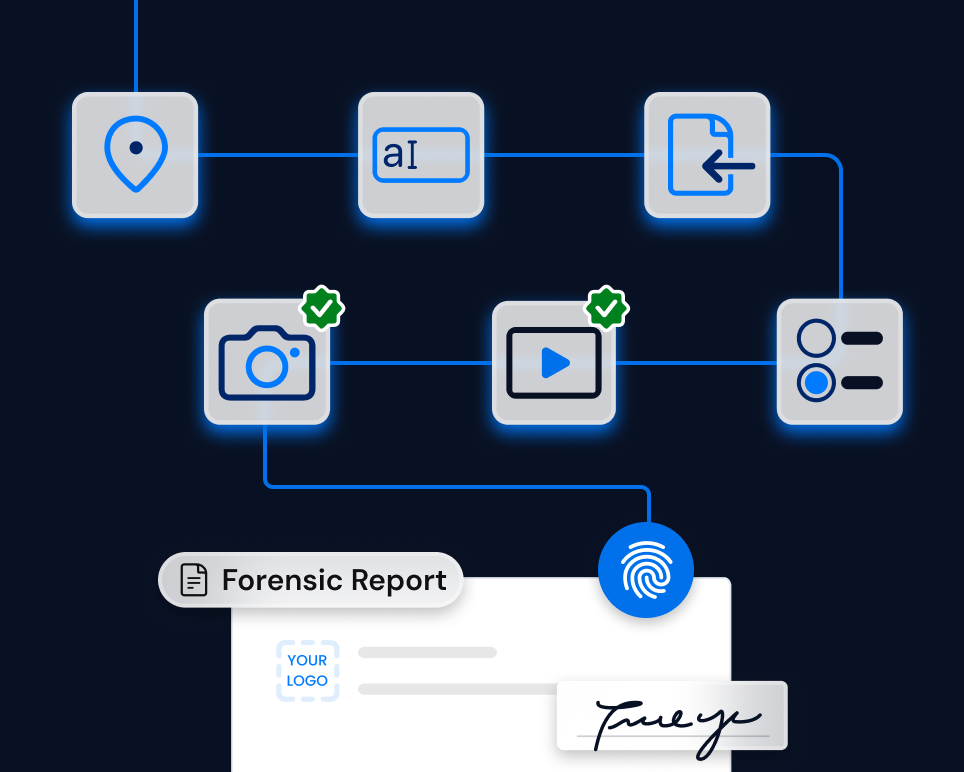
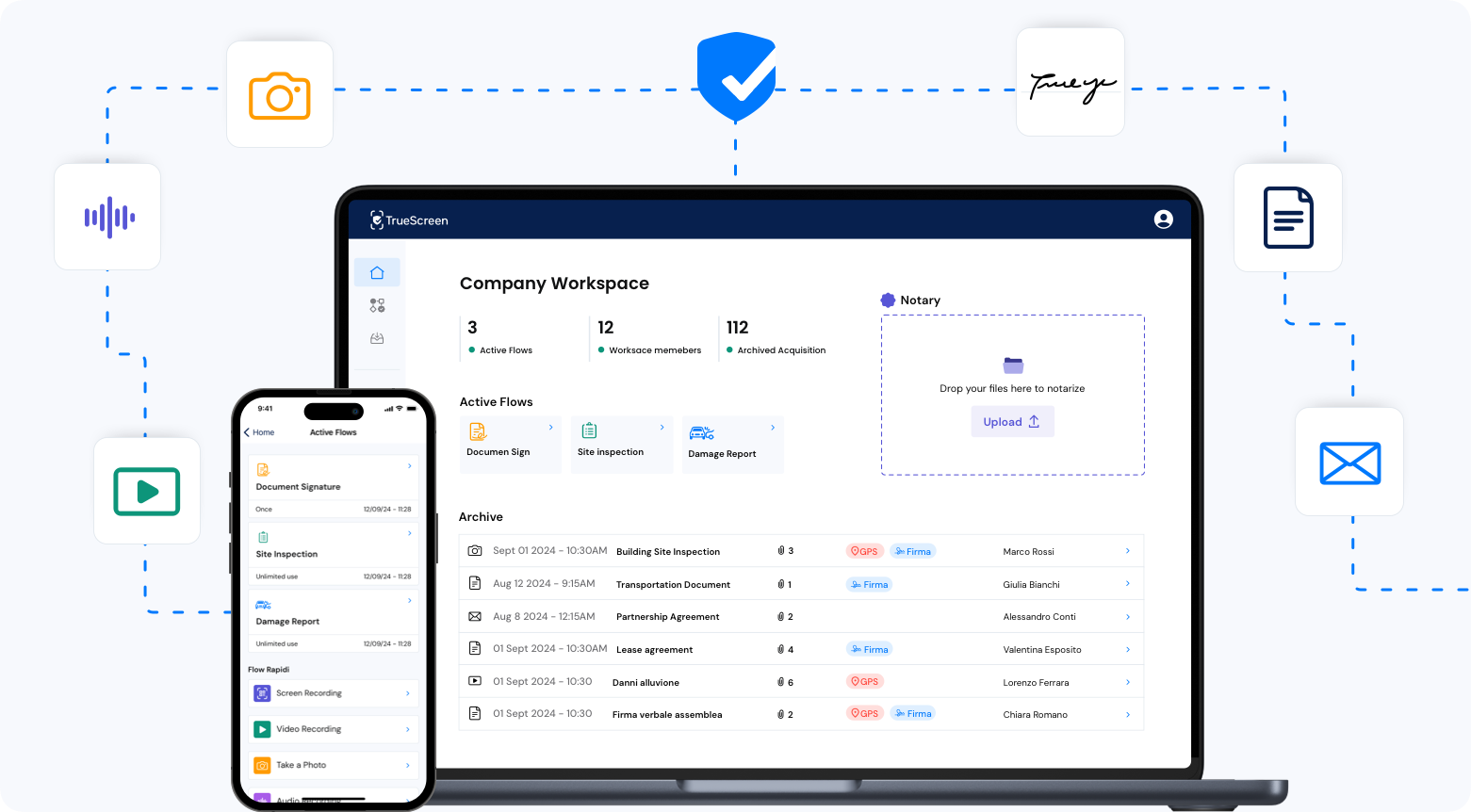
TrueScreen consente a sponsor, CRO e centri sperimentali di certificare la documentazione del trial direttamente al momento della raccolta. Ogni foto, video, documento sorgente e report di monitoraggio viene firmato digitalmente e marcato temporalmente, garantendo la conformità ai principi ALCOA+ richiesti dalle GCP.
La certificazione alla fonte assicura che ogni evidenza sia attribuibile, contemporanea e integra, semplificando le attività di verifica dei dati alla fonte e riducendo il rischio di ritrovamento durante le ispezioni regolatorie. La raccolta strutturata dei dati elimina la frammentazione documentale e produce un audit trail completo e verificabile.
Il workflow di documentazione dei trial clinici con TrueScreen è progettato per soddisfare ogni principio ALCOA+ richiesto dalle linee guida ICH E6(R3) e dal Regolamento UE 536/2014. Ogni dato acquisito è Attributable (attribuibile a un operatore identificato tramite firma digitale), Legible (leggibile e conservato in formati standard), Contemporaneous (registrato con marca temporale qualificata al momento della raccolta) e Original (acquisito alla fonte con metodologia forense che ne certifica l’integrità). L’accuratezza (Accurate) è garantita dall’impossibilità di alterare i dati dopo l’acquisizione certificata.
I principi estesi completano il framework: la completezza è assicurata dalla raccolta strutturata di ogni elemento del source data, la consistenza dalla standardizzazione del processo di documentazione dei trial clinici su tutti i centri sperimentali, la durabilità dall’archiviazione certificata con marca temporale conforme alla GCP certificazione. Ogni evidenza resta disponibile per ispezioni, audit e verifiche regolatorie, con un audit trail immutabile che documenta l’intero ciclo di monitoraggio delle sperimentazioni. Questo approccio riduce significativamente i finding durante le ispezioni delle autorità competenti e semplifica la source data verification nei siti clinici.
Cosa si certifica
Documentazione di sito
Foto e video certificati delle attività di trial site, della farmacia sperimentale, delle condizioni di conservazione del farmaco e delle aree di visita
Documenti sorgente
Acquisizione certificata di CRF, consensi informati, referti di laboratorio, diari del paziente e qualsiasi documento originale del trial
Rapporto di monitoraggio
Documentazione certificata delle visite di monitoraggio, delle verifiche in loco, delle deviazioni di protocollo e delle azioni correttive
Responsabilità del farmaco
Registrazioni certificate di ricezione, dispensazione, restituzione e distruzione del prodotto sperimentale con tracciabilità completa
Partner
Aziende farmaceutiche, CRO (Contract Research Organization), centri sperimentali, comitati etici, enti regolatori, società di consulenza regolatoria.
Integrazioni
Sistemi eTMF (Electronic Trial Master File), piattaforme EDC (Electronic Data Capture), sistemi CTMS (Clinical Trial Management System), software di farmacovigilanza, sistemi di gestione qualità.
FAQ: sperimentazioni cliniche certificato e documentazione trial
Come funziona la certificazione della documentazione dei trial clinici?
La certificazione TrueScreen è conforme alle GCP ICH E6(R3)?
3) Quali documenti del processo posso certificare?
4) Come supporta la verifica dei dati sorgente?
5) Come si integra con i sistemi eTMF ed EDC?
6) Come ridurre il rischio di trovare ispettivi?
Richiedi una demo gratuita
Parla con i nostri esperti e scopri TrueScreen per la certificazione della documentazione dei trial clinici.
